При определении степеней окисления элементов в веществах необходимо пользоваться следующими правилами:
В нейтральной молекуле степень окисления можно определить другим способом.
Задание 221). Определите степени окисления элементов в кислотах (см. табл. 14), кроме кислот
CH3COOH, HCN, HSCN.
Пример 3. Молекула
Na2Cr2O7. У натрия и кислорода постоянные степени окисления:
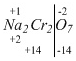
(-2) • 7 = -14;
(+1) • 2 = +2;
(+14) – (+2) = +12. Степень окисления (+12) приходится на
два атома хрома. На один атом хрома – в два раза меньше: (+12) : 2 = +6.
Нашли степень окисления хрома – (+6).
6) Степень окисления металлов (и переходных) в соединениях всегда больше нуля, так как металлы могут только отдавать электроны.
У щелочных металлов Li, Na, K, Rb, Cs, Fr степень окисления постоянная и равна (+1), так как у них всего один валентный электрон. Степень окисления элементов IIA группы также постоянная и равна (+2), степень окисления алюминия в соединениях равна (+3).
У цинка также постоянная степень окисления (+2), так как его электронная конфигурация Zn … 3s23p63d104s2, то есть третий энергетический уровень заполнен, и валентными фактически являются только электроны четвертого уровня 4s2.
Разные степени окисления имеют Cr, Mn, Fe, Cu, Sn, Pb и др.
| Элемент | Степени окисления | Устойчивые степени окисления |
| Fe | +2, +3, +6 | +3 |
| Cr | +2, +3, +6 | +3 |
| Mn | +2, +3, +6, +7 | +2, +4 |
| Cu | +1, +2 | +2 |
| Sn | +2, +4 | +2, +4 |
| Pb | +2, +4 | +2 |
7) Степень окисления элемента в кислотном остатке одинакова как в соли, так и в кислоте, поэтому иногда легче определить степень окисления в кислоте и проставить ее в соли:
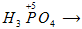
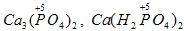
. Кислотный остаток
(PO4) одинаковый во всех солях фосфатах. Поэтому, определив степень окисления фосфора в соответствующей кислоте
H3PO4, в других соединениях просто проставляем ее над фосфором. Аналогично определим степень окисления серы в соли
Fe2(SO4)3, для чего сначала определим степень окисления серы в кислоте, где есть такой же кислотный остаток
(H2SO4). Степень окисления серы нашли (+6). Проставим ее в соли:
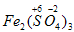
. Остается найти степень окисления железа. Так как в кислоте
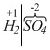
два атома водорода, то на них будет заряд (+1) • 2 = +2, следовательно,
заряд кислотного остатка (-2). Поставим этот заряд в соли:
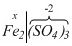
. Суммарный отрицательный заряд трех кислотных остатков:
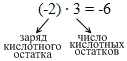
Положительных зарядов также будет шесть:
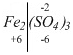
. (+6) приходится на два атома железа, а на один атом – в два раза меньше: (+6) : 2 = +3.
Пример 4. Mn(NO3)2. Определяем степень окисления азота в азотной кислоте:
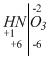
. (+6) – (+1)=+5.
Проставляем ее в соли:
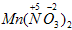
. Заряд кислотного остатка
(NO3) равен (-1), так как в молекуле
HNO3 один атом водорода:
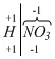
. Определим степень окисления марганца:
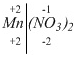
. Делим молекулу на две части, металл и кислотный остаток. Над кислотным остатком ставим заряд (-1). Умножив на число кислотных
остатков, получим сумму отрицательных зарядов (-1) • 2 = -2.
Положительных зарядов будет также два. Атомов марганца всего один,
следовательно, степень окисления его равна (+2).
Пример 5. Ca(ClO)Cl (или
CaOCl2). Это смешанная соль, в которой два кислотных остатка кислот
HClO и
HCl. Находим степень окисления хлора в них:
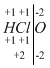
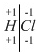
и ставим полученные степени окисления в соли:
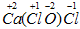
. У кальция постоянная степень окисления (+2).
Пример 6. (NH4)2CO3. Кислотный остаток
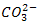
такой же как в угольной кислоте
H2CO3. Определим степень окисления углерода в ней:
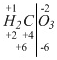
. Степень окисления
C равна (+4). Поставим ее в соль:
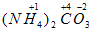
. Ион аммония
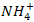
. В нем азот более электроотрицательный, чем
водород, поэтому над водородом поставим (+1), над азотом
x. Составим уравнение по правилу: сумма степеней окисления в ионе равна заряду иона.
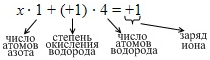 | x = +1 – 4 = -3 |
Степень окисления азота равна (-3).
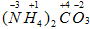
.
Пример 7. IF7. Фтор более электроотрицательный элемент, у него степень окисления в соединениях всегда (-1):
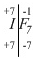
.
Делим молекулу на две части. Отрицательных степеней окисления
получилось семь, положительных должно быть тоже семь, так как заряд
молекулы равен нулю. Степень окисления йода равна (+7).
Пример 8. N2H4. Азот более электроотрицательный, поэтому ставим над водородом (+1). Делим молекулу на две части:
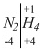
.
(-4) приходится на два атома азота, а на один атом – в два раза меньше: (-4) : 2 = (-2).
Окончательно:
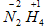
.
Пример 9. NOF. Чтобы расставить степени окисления в
этой молекуле, изобразим сначала ее структурную формулу. Так как атомы
азота, кислорода и фтора имеют 3, 2 и 1 неспаренных электронов
соответственно
(N … 2s2 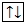 2p3,
2p3, 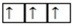 O … 2s2
O … 2s2  2p4
2p4  , F … 2s2
, F … 2s2  2p5
2p5 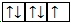 )
), то есть проявляют валентности III, II и I соответственно, то структурная формула
NOF: O = N - F,
где азот образовал три химических связи, кислород – две, а фтор – одну,
согласно числу имеющихся неспаренных электронов. Укажем направление
смещения электронных пар к более электроотрицательным атомам
O и
F:
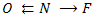
.
К атому O сместилось по двум связям 2
е, следовательно, степень окисления
O = -2.
К атому F сместился 1
е по одной связи, следовательно, степень окисления
F равна(-1).
От атома азота сместилось 3
е по трем связям, его степень окисления равна +3:
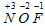
.
Задание 222). Определите степень окисления элементов в кислотах HCN и HSCN.
Пример 10. Na2[Zn(OH)4]. В этой молекуле степени окисления элементов легко расставить, не вычисляя, так как у
Na и
Zn степени окисления постоянные (+1) и (+2) соответственно, в
OH-группе степени окисления также известны
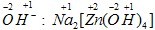
Пример 11. K3[Fe(OH)6]. В гидроксид-ионе ставим степени окисления:
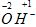
- суммарная (-1). У
K – постоянная (+1), у
Fe поставим
x и составим уравнение с одним неизвестным, считая что сумма всех степеней окисления в молекуле равна нулю:
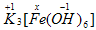
.
(+1) • 3 + x • 1 + (-1) • 6 = 0
x = 6 – 3
x = 3. Степень окисления Fe = +3.
8) В сложных соединениях степень окисления элемента тоже может быть равна нулю.
Пример 12. CH2Cl2. В этой
молекуле хлор – самый электроотрицательный элемент, он на себя тянет
электроны, принять он может только 1е до 8, до устойчивого состояния,
поэтому его степень окисления равна -1. Самый менее электроотрицательный
– водород, следовательно, его степень окисления будет положительная
(+1). Над углеродом поставим x и составим уравнение исходя из того, что сумма всех степеней окисления в молекуле равна нулю.
x • 1 + (+1) • 2 + (-1) • 2 = 0
x = 0
Структурная формула молекулы
CH2Cl2:
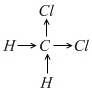
Из нее видно, что к атому углерода смещено 2е по двум связям, а по двум другим связям от него смещены 2е. 2е к нему пришли и 2е ушли, поэтому степень окисления C равна нулю.
1) Иногда расчетная степень окисления элемента не совпадает с реальной, она называется условной или кажущейся.
Пример 13. 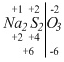
По
расчетам степень окисления серы получается (+2). Но это кажущаяся
степень окисления, так как в этой молекуле два атома серы имеют разные
степени окисления, и только суммарная получается (+2):
Пример 14. CH3COOH. Составим структурную формулу молекулы, показав смещение электронов:
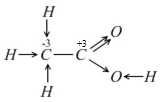
Степени окисления углерода разные (-3) и (+3). А если написать формулу по составу
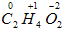
, то получим по расчетам степень окисления C равна 0. Ноль – кажущаяся степень окисления, она является средней между реальными степенями окисления (-3) и (+3).
Пример 15. 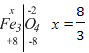
- это кажущаяся степень окисления,
так как мы знаем, что это сложный оксид
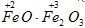
, в котором один атом железа имеет степень окисления (+2), а два других – степень окисления (+3).
Задания для закрепления
223) Определите степени окисления в веществах:
KClO3, MnCl4, MnO2, H2O2, NH4NO3, S8, K2FeO4, Pb(NO3)2, Mg3N2, NaHSO3, KMnO4, K2Cr2O7, Al(OH)SO4, PH3, CuI, CuS, Ca3(PO4)2, H2S2, NOCl, FeS2, NH2OH, Ca(H2PO4)2, Cr2(SO4)3, Mg, CS2, NCl3, (NH4)3PO4, H[AuCl4], NaHS, Fe4[Fe(CN)6]3, P4O6, Fe3[Fe(CN)6]2, FeSO3, CH3Cl, Ca(ClO2)2, CaOCl2.
224) Определите степени окисления элементов в ионах:
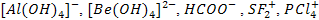
.
В какой молекуле степень окисления элемента равна нулю, а валентность - двум:
1) O2;
2) H2S;
3) P4;
4) Br2;
226) В какой молекуле степень окисления элемента равна нулю, а валентность двум:
1) P4;
2) OF2;
3) N2;
4) S8;
227) Максимально возможную степень окисления хлор проявляет в:
1) Хлорате калия;
2) Перхлорате бария;
3) Хлориде серы (IV);
4) Гипохлорите натрия;
228) Одинаковую степень окисления железо проявляет в соединениях:
1) Fe(NO3)3, FeOHCl;
2) K2FeO4, K4[Fe(CN)6];
3) FeOHSO4, K3[Fe(CN)6];
4) FePO4, FeSO4;
229) Степень окисления (-3) азот проявляет в соединении:
1) CH3NH2;
2) NH2OH;
3) NOCl;
4) KNO2;
230) Наибольшую степень окисления сера проявляет в соединении:
1) Na2S2O3;
2) BaSO3;
3) CS2;
4) Pb(HSO4)2;
231) Азот проявляет положительную степень окисления в соединениях:
1) С бромом;
2) С магнием;
3) С хлором;
4) С фтором;
232) В какой молекуле степень окисления равна нулю, а валентность четырем:
1) S8;
2) C;
3) SiH4;
4) P4;
233) Наименьшую степень окисления сера имеет:
1) K2S2;
2) COS;
3) SO2;
4) FeS2;
234) Наименьшую степень окисления хром имеет в соединении:
1) CrS;
2) CrOHSO4;
3) K2Cr2O7;
4) Na2CrO4;
§5.2. Окислительно-восстановительные реакции. Расстановка коэффициентов методом электронного баланса.
Реакции, в которых изменяются степени окисления элементов, называются окислительно-восстановительными (ОВР).
Например, горение фосфора:
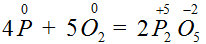
.
В ходе реакции фосфор и кислород поменяли степени окисления,
следовательно, эта реакция окислительно-восстановительная. В этом
уравнении реакции коэффициенты легко расставить обычным способом. Но
есть ОВР, где это сделать невозможно.
Один из методов расстановки коэффициентов в ОВР – метод
электронного баланса. Суть метода заключается в том, чтобы приравнять
число электронов, принимаемых окислителем, числу электронов, отдаваемых
восстановителем. Рассмотрим конкретный пример.
Пример 1. Дана схема реакции:
1) Расставим степени окисления всех элементов.
2) Определим, какие элементы изменяют степень окисления. Это атомы серы и марганца. Выпишем эти элементы отдельно.
3) Составим электронные уравнения, где показано число отданных или принятых электронов.
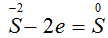
.
Степень окисления серы
повысилась в ходе реакции, следовательно,
атом 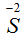 отдал отрицательные электроны. Процесс отдачи электронов записываем вычитанием.
отдал отрицательные электроны. Процесс отдачи электронов записываем вычитанием. Так как разница в зарядах
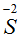
и

равна двум, то от серы ушли 2
е.
Выпишем также атомы марганца.
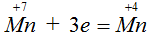
.
Степень окисления марганца понизилась с +7 до +4, следовательно,
атом 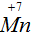 принял отрицательные электроны
принял отрицательные электроны. Так как разница в степенях окисления равна трем, то к атому
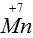
пришли 3
е. Процесс присоединения электронов записываем знаком плюс.4) Чтобы был баланс электронов, найдем наименьшее общее кратное (НОК) чисел отданных электронов (2е) и принятых (3е). НОК = 6.
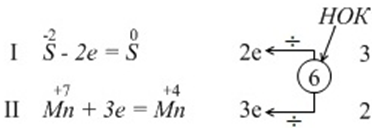
Далее делим
НОК (6) на 2
е и получим коэффициент 3
для I-го электронного уравнения и коэффициент 2 (6 : 3 = 2) для II-го
электронного уравнения с марганцем.
5) Полученные коэффициенты расставим в исходную схему реакции. Должно быть три атома
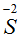
и три атома

, два атома
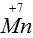
и два атома
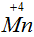
:
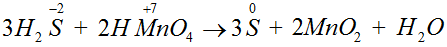
6) А далее нетрудно расставить коэффициенты обычным способом. Уравняем атомы водорода. Слева восемь атомов H, перед H2O
нужно поставить коэффициент 4, получится также восемь атомов водорода.
Кислород обычно уравнивается сам. По нему проверим правильность
расстановки коэффициентов.
3H2S + 2HMnO4 = 3S + 2MnO2 + 4H2O
Слева от знака равенства восемь атомов O, справа также восемь, значит, все сделали правильно.
Процесс отдачи электронов – это процесс окисления, а процесс присоединения электронов – это процесс восстановления.
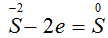 - процесс окисления.
- процесс окисления.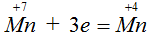 - процесс восстановления.
- процесс восстановления.Атомы
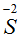
окисляются, являются восстановителями, то есть вещество
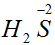
- восстановитель за счет
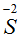
. Атомы восстанавливаются, являются окислителями, то есть вещество
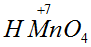
- окислитель за счет
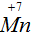
.
Восстановитель восстанавливает
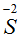
, сам при этом окисляется, и наоборот, окислитель
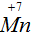
окисляет атомы
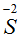
, сам при этом восстанавливается.
Оформление ОВР и расстановка коэффициентов методом электронного баланса может выглядеть так:
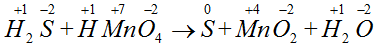
Данная реакция по типу является реакцией межмолекулярного
окисления-восстановления, так как окислитель и восстановитель – разные
атомы в разных молекулах.
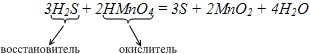
Окислитель и восстановитель всегда являются исходными
веществами, находятся в левой части уравнения, а справа – продукты
окисления-восстановления.
Пример 2. Схема реакции
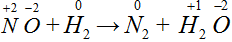
.
Составляя электронные уравнения для данной реакции,
записываем полностью двухатомные молекулы
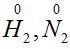
, а не отдельные атомы.
В электронном уравнении должно быть равенство числа атомов и зарядов. Число атомов уравниваем при помощи коэффициентов:
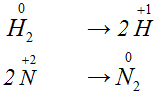
Поставив коэффициент 2 перед
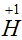
и
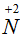
, мы таким образом уравняли число атомов. У атома
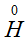
степень окисления повысилась на единицу, он отдает 1
е, но два атома водорода (
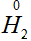
) отдают 2
е: . У атома степень окисления понизилась на две единицы, следовательно, атом принял 2
е, а два атома принимают в два раза больше:
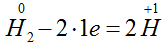
НОК = 4:
Коэффициент 2 получили для I-го электронного уравнения, умножим на два каждый член этого уравнения, тогда получается 2
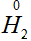
и 4
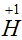
. В исходном уравнении реакции слева должно быть две молекулы
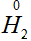
, а справа – 4 атома
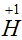
:
Коэффициент 1 мы получили для II-го электронного уравнения.
Умножим на единицу каждый член этого уравнения, то есть у нас должно
быть 2
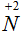
и 1
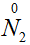
. В исходном уравнении реакции слева должно быть два атома
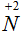
, а справа одна молекула
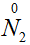
:
2NO + 2H2 = N2 + 2H2O.
Пример 3.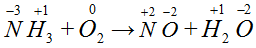
. Степени окисления меняют
N и
O.
O2 – двухатомная молекула
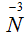

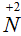
- степень окисления азота повышается, электроны уходят от атома.
Разница между степенями окисления азота (-3) и (+2) равна 5: От (-3) до 0
– три единицы и от 0 до (+2) – ещё две единицы.
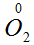

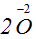
- степень окисления кислорода понижается, электроны приходят к атому
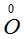
.
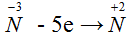
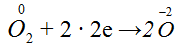 НОК
НОК = 20:
Каждый член I-го уравнения умножаем на 4. Должно быть 4 атома
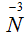
и 4 атома
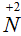
. Ставим коэффициенты для азота в исходном уравнении:
Сейчас мы должны поставить коэффициенты для атомов
кислорода. Заметим, что в уравнении встречается дважды, поэтому нельзя
ставить коэффициент перед . Достаточно поставить коэффициент 5 перед
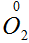
:
Коэффициент не стоит только перед H2O, следовательно, осталось уравнять число атомов водорода. Слева 12H, значит, справа поставим 6 перед H2O:
4NH3 + 5O2 = 4NO + 6H2O
Проверим по кислороду правильность расстановки коэффициентов. Слева 10 атомов O и справа 4 + 6 = 10.
Восстановитель -
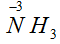
за счет
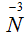
, окислитель -
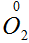
.
Не забудьте, что если степень окисления элемента
встречается в схеме реакции не один раз, а два, три раза, то
коэффициент, полученный по электронному балансу, перед таким элементом
ставить нельзя.
В схеме 191 и в
HCl, и в
PbCl2 степень окисления хлора равна (-1). В
HCl находятся все атомы хлора, часть которых меняет степень окисления до

, а часть атомов не меняет, а идет на связывание ионов
Pb2+ в
PbCl2. Коэффициент по балансу для хлора можно поставить только перед

. А далее расставлять коэффициенты обычным способом.
До сих пор мы рассматривали ОВР одного типа:
межмолекулярного окисления-восстановления, когда окислитель и
восстановитель – разные атомы и находятся в разных молекулах.
Пример 4.
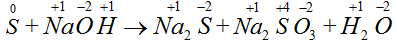
. В этой реакции степень окисления меняют только атомы серы,

присутствует в двух электронных уравнениях,
часть атомов  окисляется, а часть – восстанавливается:
окисляется, а часть – восстанавливается: 
- окислитель и

- восстановитель.
Такой тип ОВР называется реакцией диспропорционирования или самоокисления-самовосстановления. В таком случае из электронного баланса вытекает, что по I-му уравнению должно быть два атома

, и по второму уравнению один атом

, а всего три атома

. Следовательно,
когда
атом в одной и той же степени окисления встречается в двух электронных
уравнениях, то коэффициенты для него нужно складывать: 3 + NaOH
+ NaOH  2Na2S + 1Na2SO3 + H2O
2Na2S + 1Na2SO3 + H2O
Единицу в уравнение пока поставим, чтобы не забыть, что
здесь должна быть единица и не поставить на ее место другой коэффициент,
ведь уравнения бывают очень сложные. Потом, в чистовом варианте, мы
уберем эту единицу.
Далее осталось уравнять обычным способом. Сначала уравниваем
атомы натрия, а потом водорода, а по кислороду проверяем правильность
расстановки коэффициентов:
3 + 6NaOH = 2Na2S + Na2SO3 + 3H2O
+ 6NaOH = 2Na2S + Na2SO3 + 3H2O – реакция диспропорционирования.
Пример 5. 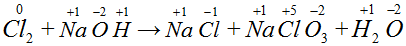
.
Степень окисления меняют только атомы хлора, эта реакция по типу ОВР
относится к реакциям диспропорционирования или
самоокисления-самовосстановления.
Электронные уравнения:
Коэффициент 5 умножим на каждый член I-го электронного уравнения, получим 5

и 10
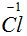
. Коэффициент 1 умножим на каждый член II-го электронного уравнения, получим 1

и 2
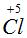
. Суммарно получается 6

. Атомы
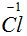
и
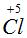
встречаются в уравнении один раз, поэтому ставим коэффициенты для них 10 и 2 в исходную схему реакции:
6Cl2 + NaOH = 10NaCl + 2NaClO3 + H2O
Далее обычным способом уравниваем атомы натрия (а водород уравнивать рано, так как в двух молекулах без коэффициентов - NaOH и H2O – имеется водород), затем водорода, а по кислороду проверяем:
6Cl2 + 12NaOH = 10NaCl + 2NaClO3 + 6H2O
Окислитель и восстановитель

.
Все полученные в уравнении коэффициенты делятся на два, поэтому окончательное уравнение:
3Cl2 + 6NaOH = 5NaCl + NaClO3 + 3H2O
Пример 6. 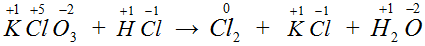
.
Еще один тип ОВР, обратный реакции диспропорционирования. Степень
окисления меняет только один элемент – хлор, высокая степень окисления
(+5) и низкая (-1) сходятся к одной степени окисления - нулю (

), степени окисления сходятся как бы на конус, отсюда
название такого типа реакции - реакция конпропорционирования, или конмутации.
Электронные уравнения:

Умножим каждый член I-го электронного уравнения на коэффициент 1, получим 2
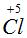
и 1

. Умножим каждый член II-го электронного уравнения на коэффициент 5, получим 10
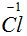
и 5

. Суммарно получим 6

. Посмотрим на исходную схему реакции. Степень окисления (-1) у хлора повторяется в
H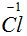
и в
K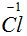
, то есть часть атомов
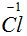
окисляются, а часть остается в неизменном виде, поэтому перед
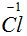
не будем пока ставить никаких коэффициентов, поставим только 6

и 2
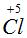
в исходную схему:
2KClO3 + HCl  6Cl2 + KCl + H2O
6Cl2 + KCl + H2O
Далее обычным способом расставляем коэффициенты. Их нет перед молекулами
HCl, KCl и
H2O. Так как хлор и водород встречаются в двух молекулах без коэффициентов (
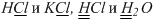
), то атомы
Cl и
H уравнивать еще рано, а вот атомы калия уже можно, он только в одной молекуле.
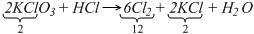
Далее уравниваем атомы хлора, так как атомы водорода еще рано уравнивать, водород находится в двух молекулах HCl и H2O, стоящих в уравнении без коэффициентов:
2KClO3 + 12HCl  6Cl2 + 2KCl + H2O
6Cl2 + 2KCl + H2O
Осталось уравнять атомы водорода, а по кислороду проверить правильность расстановки коэффициентов.
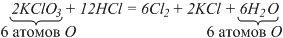
В этом уравнении все коэффициенты необходимо разделить на 2:
KClO3 + 6HCl = 3Cl2 + KCl + 3H2O
Пример 7. 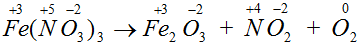
.
Степень
окисления меняют атомы азота и кислорода, находящиеся в одной молекуле,
такой тип ОВР называется реакцией внутримолекулярного
окисления-восстановления.
Электронные уравнения:
Для атома азота получился коэффициент 4, который мы не сможем поставить, так как в молекуле Fe(NO3)3 три атома . В таком случае нужно умножить I-ое электронное уравнение на 3:
Заметим, что атомы встречаются не единожды, поэтому нельзя перед ними ставить коэффициент по балансу.
Умножим каждый член I-го электронного уравнения на
полученный коэффициент 4, получаем 12 и 12 . Умножив II-е уравнение на
коэффициент 3, получим 3O2 (перед атомами балансовый коэффициент ставить нельзя).
Умножим каждый член I-го электронного уравнения на полученный коэффициент 4, получаем 12
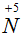
и 12
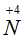
. Умножив II-е уравнение на коэффициент 3, получим 3
O2 (перед атомами балансовый коэффициент ставить нельзя).
Итак, чтобы в исходном уравнении полу чилось 12 атомов
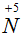
, перед молекулой
Fe(NO3)3 поставим 4:
4Fe(NO3)3  Fe2O3 + 12NO2 + 3O2.
Fe2O3 + 12NO2 + 3O2.Далее уравниваем обычным способом.
Как видим, коэффициента нет только перед молекулой Fe2O3, следовательно, уравняем атомы железа:
4Fe(NO3)3  2Fe2O3 + 12NO2 + 3O2.
2Fe2O3 + 12NO2 + 3O2.
Задания для закрепления




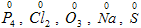
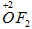 и перекисных соединений
и перекисных соединений 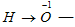
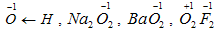 . Например:
. Например: 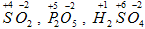
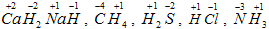 .
.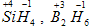 .
. 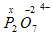 . Составим уравнение с одним неизвестным:
. Составим уравнение с одним неизвестным: 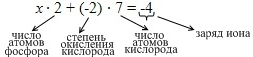
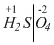 .
.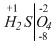 . Так как сумма всех степеней окисления равна нулю, то слева от черты поставим (+8):
. Так как сумма всех степеней окисления равна нулю, то слева от черты поставим (+8): 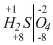 . Степень окисления водорода умножим на число атомов водорода (+1) • 2 и поставим полученную цифру (+2) под атомом водорода:
. Степень окисления водорода умножим на число атомов водорода (+1) • 2 и поставим полученную цифру (+2) под атомом водорода: 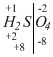 . (+8) приходится на два элемента: H и S. Сколько приходится на серу узнаем вычитанием: 8 – 2 = 6. Степень окисления серы (+6).
. (+8) приходится на два элемента: H и S. Сколько приходится на серу узнаем вычитанием: 8 – 2 = 6. Степень окисления серы (+6).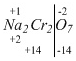
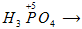
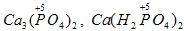 . Кислотный остаток (PO4) одинаковый во всех солях фосфатах. Поэтому, определив степень окисления фосфора в соответствующей кислоте H3PO4, в других соединениях просто проставляем ее над фосфором. Аналогично определим степень окисления серы в соли Fe2(SO4)3, для чего сначала определим степень окисления серы в кислоте, где есть такой же кислотный остаток (H2SO4). Степень окисления серы нашли (+6). Проставим ее в соли:
. Кислотный остаток (PO4) одинаковый во всех солях фосфатах. Поэтому, определив степень окисления фосфора в соответствующей кислоте H3PO4, в других соединениях просто проставляем ее над фосфором. Аналогично определим степень окисления серы в соли Fe2(SO4)3, для чего сначала определим степень окисления серы в кислоте, где есть такой же кислотный остаток (H2SO4). Степень окисления серы нашли (+6). Проставим ее в соли: 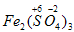 . Остается найти степень окисления железа. Так как в кислоте
. Остается найти степень окисления железа. Так как в кислоте 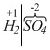 два атома водорода, то на них будет заряд (+1) • 2 = +2, следовательно,
заряд кислотного остатка (-2). Поставим этот заряд в соли:
два атома водорода, то на них будет заряд (+1) • 2 = +2, следовательно,
заряд кислотного остатка (-2). Поставим этот заряд в соли: 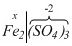 . Суммарный отрицательный заряд трех кислотных остатков:
. Суммарный отрицательный заряд трех кислотных остатков:
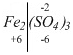 . (+6) приходится на два атома железа, а на один атом – в два раза меньше: (+6) : 2 = +3.
. (+6) приходится на два атома железа, а на один атом – в два раза меньше: (+6) : 2 = +3.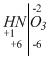 . (+6) – (+1)=+5.
Проставляем ее в соли:
. (+6) – (+1)=+5.
Проставляем ее в соли: 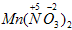 . Заряд кислотного остатка (NO3) равен (-1), так как в молекуле HNO3 один атом водорода:
. Заряд кислотного остатка (NO3) равен (-1), так как в молекуле HNO3 один атом водорода: 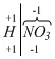 . Определим степень окисления марганца:
. Определим степень окисления марганца: 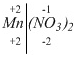 . Делим молекулу на две части, металл и кислотный остаток. Над кислотным остатком ставим заряд (-1). Умножив на число кислотных
. Делим молекулу на две части, металл и кислотный остаток. Над кислотным остатком ставим заряд (-1). Умножив на число кислотных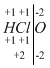
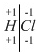 и ставим полученные степени окисления в соли:
и ставим полученные степени окисления в соли: 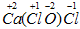 . У кальция постоянная степень окисления (+2).
. У кальция постоянная степень окисления (+2).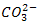 такой же как в угольной кислоте H2CO3. Определим степень окисления углерода в ней:
такой же как в угольной кислоте H2CO3. Определим степень окисления углерода в ней: 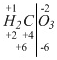 . Степень окисления C равна (+4). Поставим ее в соль:
. Степень окисления C равна (+4). Поставим ее в соль: 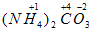 . Ион аммония
. Ион аммония 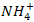 . В нем азот более электроотрицательный, чем
. В нем азот более электроотрицательный, чем 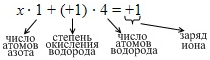
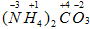 .
.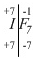 .
.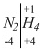 .
.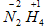 .
. 2p3,
2p3,  O … 2s2
O … 2s2  2p4
2p4  , F … 2s2
, F … 2s2  2p5
2p5  ), то есть проявляют валентности III, II и I соответственно, то структурная формула NOF: O = N - F,
где азот образовал три химических связи, кислород – две, а фтор – одну,
согласно числу имеющихся неспаренных электронов. Укажем направление
смещения электронных пар к более электроотрицательным атомам O и F:
), то есть проявляют валентности III, II и I соответственно, то структурная формула NOF: O = N - F,
где азот образовал три химических связи, кислород – две, а фтор – одну,
согласно числу имеющихся неспаренных электронов. Укажем направление
смещения электронных пар к более электроотрицательным атомам O и F: 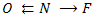 . К атому O сместилось по двум связям 2е, следовательно, степень окисления O = -2. К атому F сместился 1е по одной связи, следовательно, степень окисления F равна(-1). От атома азота сместилось 3е по трем связям, его степень окисления равна +3:
. К атому O сместилось по двум связям 2е, следовательно, степень окисления O = -2. К атому F сместился 1е по одной связи, следовательно, степень окисления F равна(-1). От атома азота сместилось 3е по трем связям, его степень окисления равна +3: 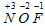 .
.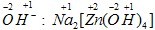
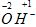 - суммарная (-1). У K – постоянная (+1), у Fe поставим x и составим уравнение с одним неизвестным, считая что сумма всех степеней окисления в молекуле равна нулю:
- суммарная (-1). У K – постоянная (+1), у Fe поставим x и составим уравнение с одним неизвестным, считая что сумма всех степеней окисления в молекуле равна нулю: 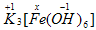 .
.
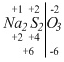
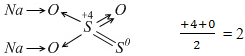
 Степени окисления углерода разные (-3) и (+3). А если написать формулу по составу
Степени окисления углерода разные (-3) и (+3). А если написать формулу по составу 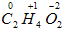 , то получим по расчетам степень окисления C равна 0. Ноль – кажущаяся степень окисления, она является средней между реальными степенями окисления (-3) и (+3).
, то получим по расчетам степень окисления C равна 0. Ноль – кажущаяся степень окисления, она является средней между реальными степенями окисления (-3) и (+3).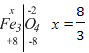 - это кажущаяся степень окисления,
- это кажущаяся степень окисления,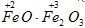 , в котором один атом железа имеет степень окисления (+2), а два других – степень окисления (+3).
, в котором один атом железа имеет степень окисления (+2), а два других – степень окисления (+3). 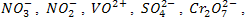
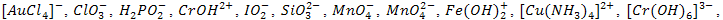

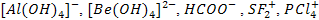 .
.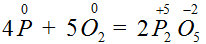 .
.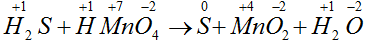
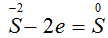 . Степень окисления серы повысилась в ходе реакции, следовательно, атом
. Степень окисления серы повысилась в ходе реакции, следовательно, атом 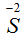 отдал отрицательные электроны. Процесс отдачи электронов записываем вычитанием. Так как разница в зарядах
отдал отрицательные электроны. Процесс отдачи электронов записываем вычитанием. Так как разница в зарядах 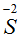 и
и  равна двум, то от серы ушли 2е.
равна двум, то от серы ушли 2е.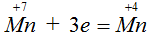 . Степень окисления марганца понизилась с +7 до +4, следовательно, атом
. Степень окисления марганца понизилась с +7 до +4, следовательно, атом 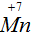 принял отрицательные электроны. Так как разница в степенях окисления равна трем, то к атому
принял отрицательные электроны. Так как разница в степенях окисления равна трем, то к атому 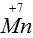 пришли 3е. Процесс присоединения электронов записываем знаком плюс.
пришли 3е. Процесс присоединения электронов записываем знаком плюс.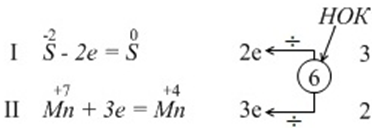 Далее делим НОК (6) на 2е и получим коэффициент 3
для I-го электронного уравнения и коэффициент 2 (6 : 3 = 2) для II-го
электронного уравнения с марганцем.
Далее делим НОК (6) на 2е и получим коэффициент 3
для I-го электронного уравнения и коэффициент 2 (6 : 3 = 2) для II-го
электронного уравнения с марганцем.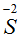 и три атома
и три атома  , два атома
, два атома 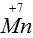 и два атома
и два атома 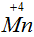 :
: 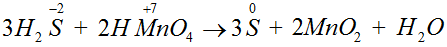
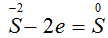 - процесс окисления.
- процесс окисления.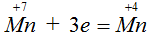 - процесс восстановления.
- процесс восстановления.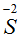 окисляются, являются восстановителями, то есть вещество
окисляются, являются восстановителями, то есть вещество 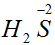 - восстановитель за счет
- восстановитель за счет 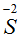 . Атомы восстанавливаются, являются окислителями, то есть вещество
. Атомы восстанавливаются, являются окислителями, то есть вещество 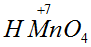 - окислитель за счет
- окислитель за счет 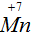 .
.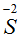 , сам при этом окисляется, и наоборот, окислитель
, сам при этом окисляется, и наоборот, окислитель 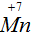 окисляет атомы
окисляет атомы 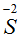 , сам при этом восстанавливается.
, сам при этом восстанавливается.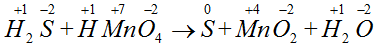
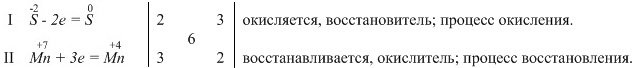
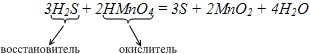
 H3PO4 + HCl;
H3PO4 + HCl; HNO3 + HCl;
HNO3 + HCl; KNO3 + KCl + H2O;
KNO3 + KCl + H2O; H3PO4 + MnO2 + H2O;
H3PO4 + MnO2 + H2O;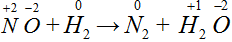 . Составляя электронные уравнения для данной реакции, записываем полностью двухатомные молекулы
. Составляя электронные уравнения для данной реакции, записываем полностью двухатомные молекулы 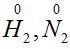 , а не отдельные атомы. В электронном уравнении должно быть равенство числа атомов и зарядов. Число атомов уравниваем при помощи коэффициентов:
, а не отдельные атомы. В электронном уравнении должно быть равенство числа атомов и зарядов. Число атомов уравниваем при помощи коэффициентов: 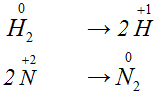
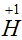 и
и 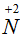 , мы таким образом уравняли число атомов. У атома
, мы таким образом уравняли число атомов. У атома 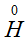 степень окисления повысилась на единицу, он отдает 1е, но два атома водорода (
степень окисления повысилась на единицу, он отдает 1е, но два атома водорода (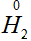 ) отдают 2е: . У атома степень окисления понизилась на две единицы, следовательно, атом принял 2е, а два атома принимают в два раза больше:
) отдают 2е: . У атома степень окисления понизилась на две единицы, следовательно, атом принял 2е, а два атома принимают в два раза больше: 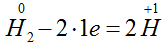
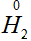 и 4
и 4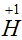 . В исходном уравнении реакции слева должно быть две молекулы
. В исходном уравнении реакции слева должно быть две молекулы 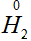 , а справа – 4 атома
, а справа – 4 атома 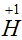 :
: 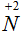 и 1
и 1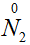 . В исходном уравнении реакции слева должно быть два атома
. В исходном уравнении реакции слева должно быть два атома 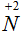 , а справа одна молекула
, а справа одна молекула 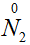 :
: 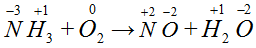 . Степени окисления меняют N и O. O2 – двухатомная молекула
. Степени окисления меняют N и O. O2 – двухатомная молекула 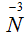

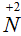 - степень окисления азота повышается, электроны уходят от атома.
Разница между степенями окисления азота (-3) и (+2) равна 5: От (-3) до 0
– три единицы и от 0 до (+2) – ещё две единицы.
- степень окисления азота повышается, электроны уходят от атома.
Разница между степенями окисления азота (-3) и (+2) равна 5: От (-3) до 0
– три единицы и от 0 до (+2) – ещё две единицы.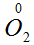

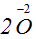 - степень окисления кислорода понижается, электроны приходят к атому
- степень окисления кислорода понижается, электроны приходят к атому 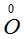 .
.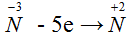
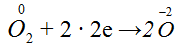
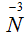 и 4 атома
и 4 атома 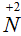 . Ставим коэффициенты для азота в исходном уравнении:
. Ставим коэффициенты для азота в исходном уравнении: 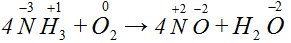
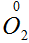 :
: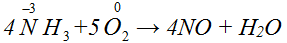
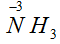 за счет
за счет 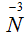 , окислитель -
, окислитель - 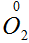 .
. Cu + N2 + H2O;
Cu + N2 + H2O; HBrO3 + HCl;
HBrO3 + HCl; S + I2 + H2O;
S + I2 + H2O; PbCl2 + Cl2 + H2O;
PbCl2 + Cl2 + H2O; MnCl2 + Cl2 + KCl + H2O;
MnCl2 + Cl2 + KCl + H2O; , а часть атомов не меняет, а идет на связывание ионов Pb2+ в PbCl2. Коэффициент по балансу для хлора можно поставить только перед
, а часть атомов не меняет, а идет на связывание ионов Pb2+ в PbCl2. Коэффициент по балансу для хлора можно поставить только перед  . А далее расставлять коэффициенты обычным способом.
. А далее расставлять коэффициенты обычным способом. 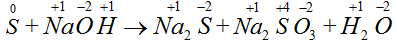 . В этой реакции степень окисления меняют только атомы серы,
. В этой реакции степень окисления меняют только атомы серы,  присутствует в двух электронных уравнениях, часть атомов
присутствует в двух электронных уравнениях, часть атомов  окисляется, а часть – восстанавливается:
окисляется, а часть – восстанавливается: 
 - окислитель и
- окислитель и  - восстановитель. Такой тип ОВР называется реакцией диспропорционирования или самоокисления-самовосстановления.
- восстановитель. Такой тип ОВР называется реакцией диспропорционирования или самоокисления-самовосстановления.  , и по второму уравнению один атом
, и по второму уравнению один атом  , а всего три атома
, а всего три атома  . Следовательно, когда
атом в одной и той же степени окисления встречается в двух электронных
уравнениях, то коэффициенты для него нужно складывать:
. Следовательно, когда
атом в одной и той же степени окисления встречается в двух электронных
уравнениях, то коэффициенты для него нужно складывать:  + NaOH
+ NaOH  2Na2S + 1Na2SO3 + H2O
2Na2S + 1Na2SO3 + H2O + 6NaOH = 2Na2S + Na2SO3 + 3H2O – реакция диспропорционирования.
+ 6NaOH = 2Na2S + Na2SO3 + 3H2O – реакция диспропорционирования.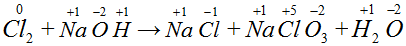 .
Степень окисления меняют только атомы хлора, эта реакция по типу ОВР
относится к реакциям диспропорционирования или
самоокисления-самовосстановления.
.
Степень окисления меняют только атомы хлора, эта реакция по типу ОВР
относится к реакциям диспропорционирования или
самоокисления-самовосстановления. 
 и 10
и 10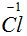 . Коэффициент 1 умножим на каждый член II-го электронного уравнения, получим 1
. Коэффициент 1 умножим на каждый член II-го электронного уравнения, получим 1 и 2
и 2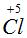 . Суммарно получается 6
. Суммарно получается 6 . Атомы
. Атомы 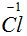 и
и 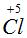 встречаются в уравнении один раз, поэтому ставим коэффициенты для них 10 и 2 в исходную схему реакции:
встречаются в уравнении один раз, поэтому ставим коэффициенты для них 10 и 2 в исходную схему реакции:  .
. PH3 + NaH2PO2;
PH3 + NaH2PO2; HBr + HBrO3;
HBr + HBrO3; HMnO4 + MnO2 + H2O;
HMnO4 + MnO2 + H2O; KCl + KClO3;
KCl + KClO3; Cl2 + HClO3 + H2O;
Cl2 + HClO3 + H2O; HNO2 + HNO3;
HNO2 + HNO3; BaI2 + Ba(IO3)2 + H2O;
BaI2 + Ba(IO3)2 + H2O;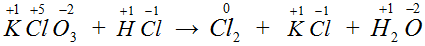 .
Еще один тип ОВР, обратный реакции диспропорционирования. Степень
окисления меняет только один элемент – хлор, высокая степень окисления
(+5) и низкая (-1) сходятся к одной степени окисления - нулю (
.
Еще один тип ОВР, обратный реакции диспропорционирования. Степень
окисления меняет только один элемент – хлор, высокая степень окисления
(+5) и низкая (-1) сходятся к одной степени окисления - нулю (  ), степени окисления сходятся как бы на конус, отсюда название такого типа реакции - реакция конпропорционирования, или конмутации.
), степени окисления сходятся как бы на конус, отсюда название такого типа реакции - реакция конпропорционирования, или конмутации.
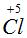 и 1
и 1 . Умножим каждый член II-го электронного уравнения на коэффициент 5, получим 10
. Умножим каждый член II-го электронного уравнения на коэффициент 5, получим 10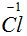 и 5
и 5 . Суммарно получим 6
. Суммарно получим 6 . Посмотрим на исходную схему реакции. Степень окисления (-1) у хлора повторяется в H
. Посмотрим на исходную схему реакции. Степень окисления (-1) у хлора повторяется в H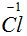 и в K
и в K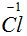 , то есть часть атомов
, то есть часть атомов 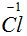 окисляются, а часть остается в неизменном виде, поэтому перед
окисляются, а часть остается в неизменном виде, поэтому перед 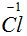 не будем пока ставить никаких коэффициентов, поставим только 6
не будем пока ставить никаких коэффициентов, поставим только 6 и 2
и 2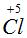 в исходную схему:
в исходную схему:  6Cl2 + KCl + H2O
6Cl2 + KCl + H2O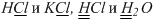 ), то атомы Cl и H уравнивать еще рано, а вот атомы калия уже можно, он только в одной молекуле.
), то атомы Cl и H уравнивать еще рано, а вот атомы калия уже можно, он только в одной молекуле.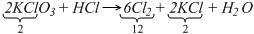
 6Cl2 + 2KCl + H2O
6Cl2 + 2KCl + H2O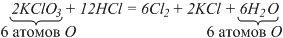
 S + H2O;
S + H2O; PCl3;
PCl3; FeO;
FeO; P2O3;
P2O3; MnO2
MnO2 + K2SO4 + H2SO4;
+ K2SO4 + H2SO4;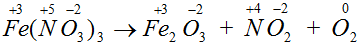 . Степень
окисления меняют атомы азота и кислорода, находящиеся в одной молекуле,
такой тип ОВР называется реакцией внутримолекулярного
окисления-восстановления.
. Степень
окисления меняют атомы азота и кислорода, находящиеся в одной молекуле,
такой тип ОВР называется реакцией внутримолекулярного
окисления-восстановления.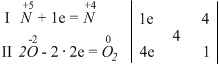

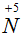 и 12
и 12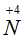 . Умножив II-е уравнение на коэффициент 3, получим 3O2 (перед атомами балансовый коэффициент ставить нельзя).
. Умножив II-е уравнение на коэффициент 3, получим 3O2 (перед атомами балансовый коэффициент ставить нельзя). 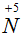 , перед молекулой Fe(NO3)3 поставим 4: 4Fe(NO3)3
, перед молекулой Fe(NO3)3 поставим 4: 4Fe(NO3)3  Fe2O3 + 12NO2 + 3O2.
Fe2O3 + 12NO2 + 3O2. 2Fe2O3 + 12NO2 + 3O2.
2Fe2O3 + 12NO2 + 3O2. KCl + O2;
KCl + O2; K2MnO4 + O2 + H2O;
K2MnO4 + O2 + H2O; KCl + O2;
KCl + O2; MnO2 + NO2;
MnO2 + NO2; Cr2O3 +O2 +K2CrO4;
Cr2O3 +O2 +K2CrO4; Cu(NO3)2 + NO + H2O
Cu(NO3)2 + NO + H2O Fe(OH)3
Fe(OH)3 KBr + KBrO3 + H2O
KBr + KBrO3 + H2O MgSO4 + H2S + H2O
MgSO4 + H2S + H2O Br2 + CrBr3 + KBr + H2O
Br2 + CrBr3 + KBr + H2O Na2MnO4 + O2 + H2O
Na2MnO4 + O2 + H2O Ca(NO3)2 + NH4NO3 + H2O
Ca(NO3)2 + NH4NO3 + H2O Cr2(SO4)3 + Na2SO4 + K2SO4 + H2O
Cr2(SO4)3 + Na2SO4 + K2SO4 + H2O Fe2(SO4)3 + NO + H2O
Fe2(SO4)3 + NO + H2O Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
Fe2(SO4)3 + MnSO4 + K2SO4 + H2O Na2CrO4 + NaCl + H2O
Na2CrO4 + NaCl + H2O